日本冬虫夏草の安全性について
日本冬虫夏草は東北大学大学院の薬学研究科によるマウスを対象とした亜急性毒性試験で安全性が確認されています。
亜急性毒性試験とは1ヵ月から3ヵ月程度の期間で実験動物に被験対象物質を曝露させ続けて、生存率や症状、血液学、生化学、病理学に基づいて被験対象物質の毒性影響を評価する試験方法です。
N.M.I自然薬食微生物研究所所長の矢萩信夫氏から提供された日本冬虫夏草の培養上清液冷凍乾燥粉末を4つのグループ分けした5-6週齢の雄性マウスに経口摂取させ、体重変動、血液状態、臓器重量、肝逸脱酵素などを測定し亜急性毒性の評価を行った。
グループは10-11匹を1グループとして、日本冬虫夏草の培養上清液をそれぞれ高量,中量,少量(100,10,1 mg/kg/day)に調整して毎日17時に投与する3グループと上清液の溶剤である生理食塩水のみを投与した1グループに分けて試験を行った。
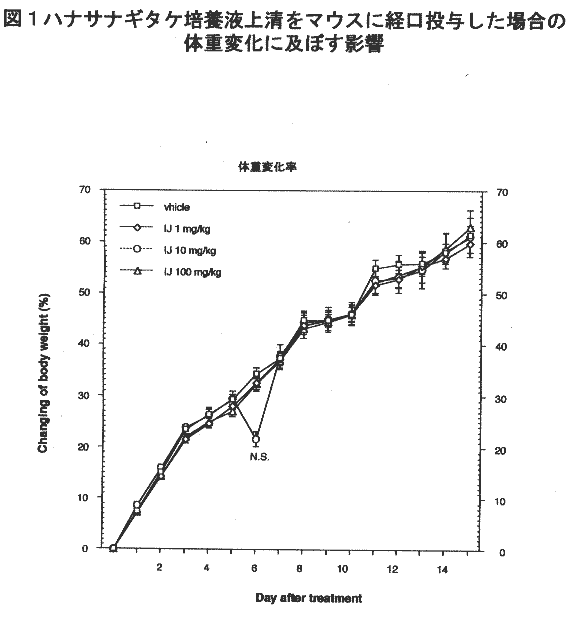
体重変動:1日1度生理食塩水を投与する前に検体の体重を測定した。
検体の体重は群によってばらつきがある為、各群の投与開始初日の体重の平均を1として、この値に対する増減値で評価を行う。
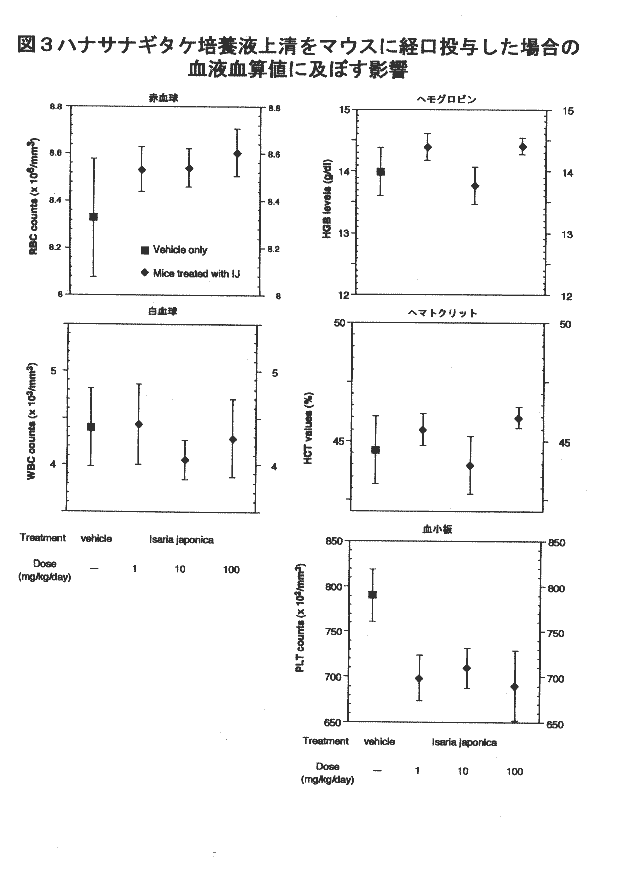
血液状態:2週間の投与終了後に採血を行い血中の赤血球数(RBC)白血球数(WBC)ヘマトクリット値(HCT)ヘモグロビン値(HGB)血小板数(PLT)の数値を評価する。
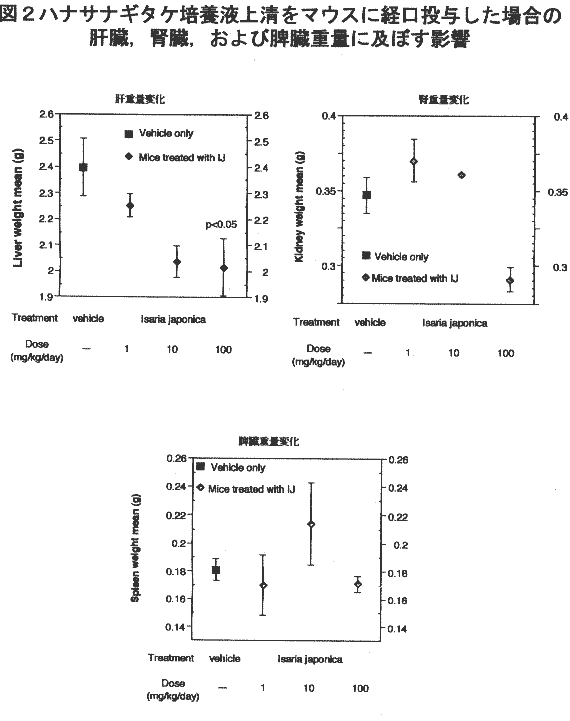
臓器重量:期間終了時の採血後に剖検を行い肝臓、脾臓、腎臓などの重量を測定する。
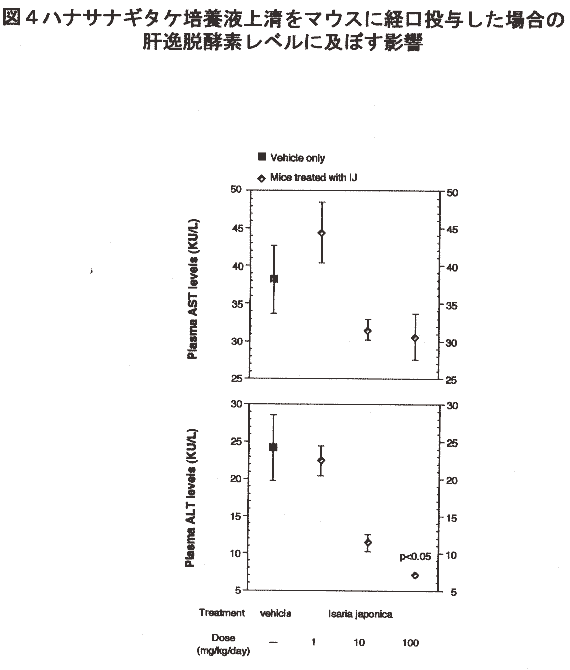
肝逸脱酵素の測定:肝逸脱酵素の測定は薬物の安全性を評価する上でもっとも普遍的に用いられる項目です。
期間終了時に採血した血液の一部を遠心した血漿の、肝逸脱酵素(ALTとAST)の活性を測定する。
対象の毒性が強い場合、解毒の過程で肝実質細胞は壊死して肝逸脱酵素レベルが低下し、毒性が低ければ肝逸脱酵素レベルが高まる傾向が見られます。
上記の評価項目を実験開始前後のグループの平均値からみて±標準誤差で表示し、分散分析による多重検定によって薬理統計学的有意差の算出を行い5%を超える乖離が認められた場合に有意差があるとして判定を行う。
体重変動:体重の変動は投与したグループと非投与のグループと差異は見られなかった。
血液状態:期間後の血算値を調べた結果、白血球数、ヘモグロビン、およびヘマトクリットレベルは全く差は無かった。
赤血球数は全ての投与グループにて僅かに増加したが有意差は認められなかった。
血小板数は全ての投与グループにて僅かに減少したが有意差は認められなかった。
臓器重量:期間後に剖検した胃、十二指腸、小腸、大腸などの臓器には全てのグループで肉眼的な異常所見は見られず、毒性が端的に現れる臓器の肝臓、脾臓、腎臓などの湿重量は100mg/kg/dayのグループで肝臓と腎臓に僅かな萎縮が見られたが、脾臓には萎縮は認められなかった。
臓器の炎症が起きた場合に確認される腫脹や鬱血なども認められず、胆嚢異常や脂質代謝の異常を示す胆嚢内の胆汁混濁も認められなかった。
肝逸脱酵素の測定:投与を行ったグループと非投与のグループで肝逸脱酵素の血中レベルの変動は見られなかった。
上記の検査結果から日本冬虫夏草は全ての評価項目で危険性は認められなかった。
本実験でマウスに与えた培養上清液はヒトに換算した場合、高用量投与群で大人が1日に4.5L~5Lを服用した場合に相当(100mg/kg/dayのグループの場合)するため、ヒトでは現実性のない高用量でも摂取した際でも危険性は薄いと考えられ、日本冬虫夏草の培養上清液には急性・亜急性毒性試験において毒性は認められないと結論付けられた。
(本実験終了後も高用量投与群の経過観察を続けたが、急性的な致死や衰弱は認められませんでした。)
 |
 |
 |
 |














